+Gonzalo Alvear+
En esta entrada presentamos una guía de consenso sobre el diagnóstico diferencial de las exacerbaciones en pacientes con EPOC.

Am J Respir Crit Care Med 2023;207:1134–1144
Introducción
Las exacerbaciones de la EPOC (EA) empeoran el estado de salud, aceleran la declinación de la función pulmonar y aumentan el riesgo de nuevas EA, hospitalizaciones y muerte.
Los pacientes con EPOC son generalmente añosos y tienen múltiples comorbilidades, incluyendo la insuficiencia cardiaca (IC), enfermedad cardiaca isquémica (ECI), arritmias, enfermedad pulmonar intersticial (EPI), bronquiectasias, ansiedad y depresión, todas las cuales aumentan el riesgo de EA y muerte. Además, la incidencia de neumonías, neumotórax y embolia pulmonar (EP), las que pueden imitar o empeorar una EA, son frecuentes en estos pacientes. Aproximadamente entre el 25%-65% de los pacientes hospitalizados por una EA mueren dentro de 1 y 5 años, respectivamente, debido principalmente a complicaciones respiratorias o cardiovasculares, con cerca del 20% que se rehospitaliza dentro de los 30 días después del alta. Cerca del 70% de estas rehospitalizaciones, se deben a descompensación de otras comorbilidades.
Se ha propuesto una nueva definición de las EA que, además del empeoramiento de los síntomas, incorpora mediciones objetivas de seis variables (frecuencias respiratoria y cardiaca, saturación de oxígeno, disnea, proteína C reactiva (PCR) y, cuando se pueda, gases en sangre arterial) para determinar la severidad de la EA. La mayoría de los casos severos de EA que se ven en los servicios de urgencias se acompañan de descompensación de comorbilidades (particularmente IC) o el desarrollo nuevas morbilidades (por ejemplo, EP o neumonía), las que pueden confundirse o contribuir a una EA.
Esta revisión provee al clínico de un enfoque práctico de los pacientes con EPOC que se presentan con empeoramiento de sus síntomas, particularmente la disnea, no explicados por una EA, que acuden al servicio de urgencia.
Métodos
Este es un consenso de los mismos expertos que propusieron la nueva definición y clasificación de severidad de la EA de Roma, incluyendo ahora a expertos de Europa y Sudamérica.
En este documento, se define a los pacientes con EPOC confirmada por espirometría o, si no hay confirmación espirométrica, por la historia de exposición al tabaquismo y/o a contaminantes ambientales, síntomas respiratorios crónicos y/o pacientes que están recibiendo terapia farmacológica para la EPOC.
Evaluación inicial
Una cuidadosa historia clínica y examen físico, complementados con las mediciones razonables de variables objetivables, puede ayudar a establecer, con bastante grado de certeza, que una EA es el diagnóstico más probable (Tabla 1). Pero en muchos pacientes, los signos y síntomas de una EA (especialmente cuando es más severa) no son específicos, y otras enfermedades pueden imitar una EA y/o agravar su presentación clínica (Figura 1). Se desarrolló un algoritmo práctico inicial para ayudar a buscar un diagnóstico más preciso (Figura 2).

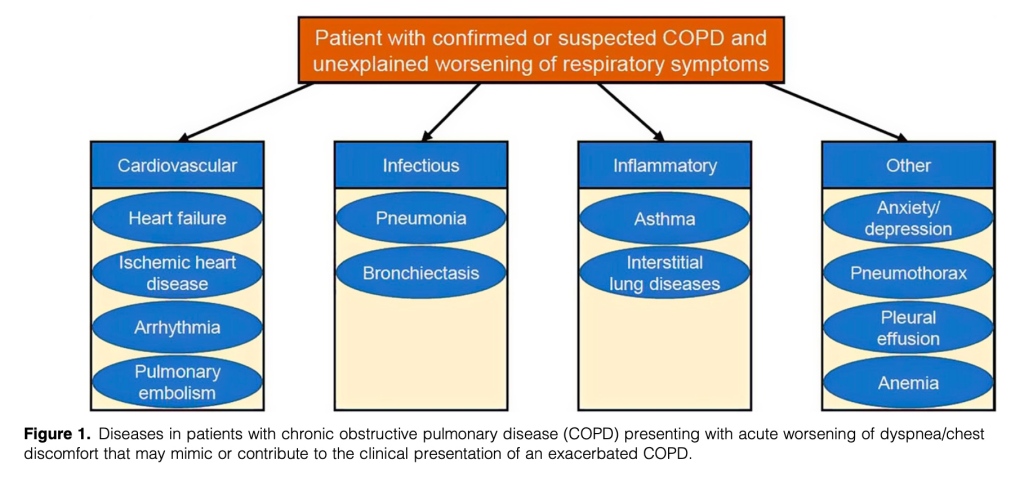
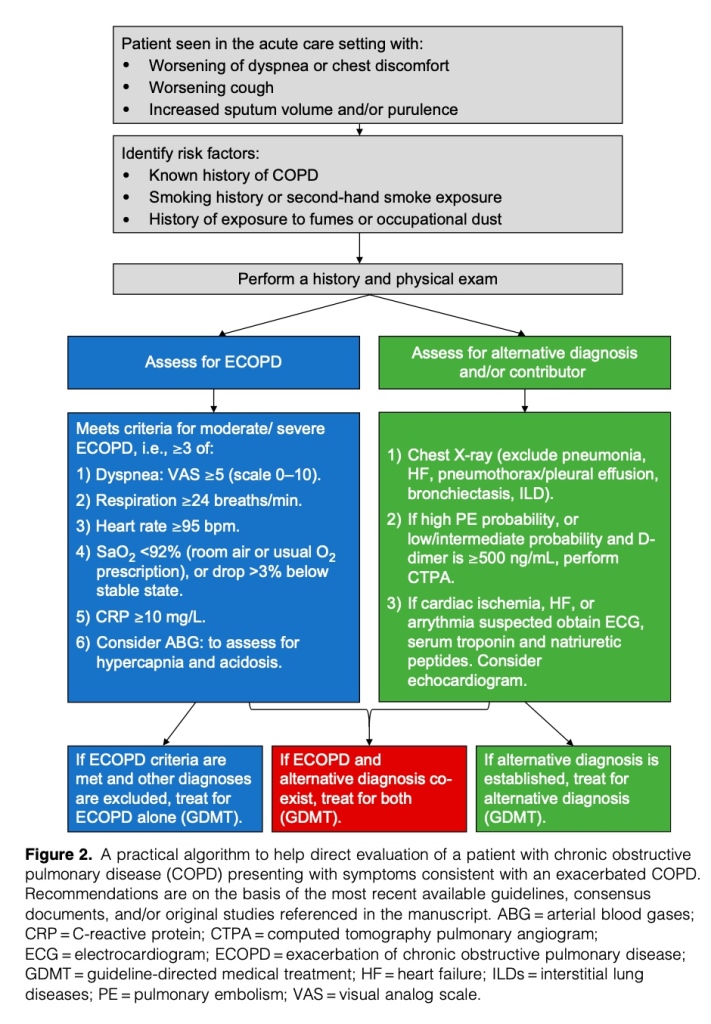
Morbilidades cardiovasculares
Las morbilidades cardiovasculares están frecuentemente presentes en los pacientes que experimentan una EA, por lo que la historia clínica es importante en estos casos para evaluar su presencia e impacto.
– IC aguda
La IC aguda se define como el empeoramiento de la disnea en reposo (particularmente estando en posición supina) o durante el ejercicio y/o fatiga, junto con signos de retención de líquido, con evidencia objetiva de alteración de la estructura o función del corazón. La EPOC está presente en hasta el 50% de los pacientes con IC y la IC ocurre en cerca del 20% de los individuos con EPOC, debido a factores de riesgo comunes (envejecimiento y tabaquismo) y mecanismos subyacentes que se superponen (inflamación sistémica, disfunción endotelial y atrofia muscular). Además, el diagnóstico de IC es difícil de confirmar en los pacientes con fracción de eyección conservada, lo que es común en los individuos con EPOC. La hipoxemia y taquicardia en la EPOC pueden promover la descompensación de la IC, mientras que la congestión pulmonar en la IC puede empeorar la obstrucción de la vía aérea. Además, las sibilancias son comunes en la IC aguda (aproximadamente en el 30%), mientras que la EPOC puede enmascarar la presencia de crepitaciones bibasales. Pero su presencia, junto con la evidencia de edema de extremidades inferiores, presión elevada de la yugular y un tercer ruido cardiaco, aumentan la probabilidad de que la IC sea la causa o un contribuyente al evento agudo.
La radiografía de tórax puede ayudar a distinguir una EA de la IC aguda, con la presencia de cardiomegalia como apoyo del daño estructural del corazón y de edema pulmonar. Los mejores marcadores de laboratorio de la IC son los péptidos natriuréticos, los que, si están elevados, apoyan también el diagnóstico de IC aguda (Figura 3). Pero hay que tener en cuenta que los péptidos natriuréticos están comúnmente elevados en pacientes con EPOC estable o neumonía y aumentan aún más en los pacientes con EA, incluso sin IC aguda. Más útil es cuando los niveles de los péptidos natriuréticos están bajos, ya que tienen un valor predictivo negativo excelente para la IC aguda, incluso en pacientes con EA. Los pacientes con EA y péptidos natriuréticos elevados tienen peor pronóstico, incluyendo el riesgo de muerte. La ultrasonografía puede ayudar a diferenciar la EA de la IC aguda, aunque se requiere de más estudios para establecer su impacto sobre desenlaces beneficiosos. La figura 3 muestra un algoritmo diagnóstico para evaluar a pacientes con sospecha de IC aguda.
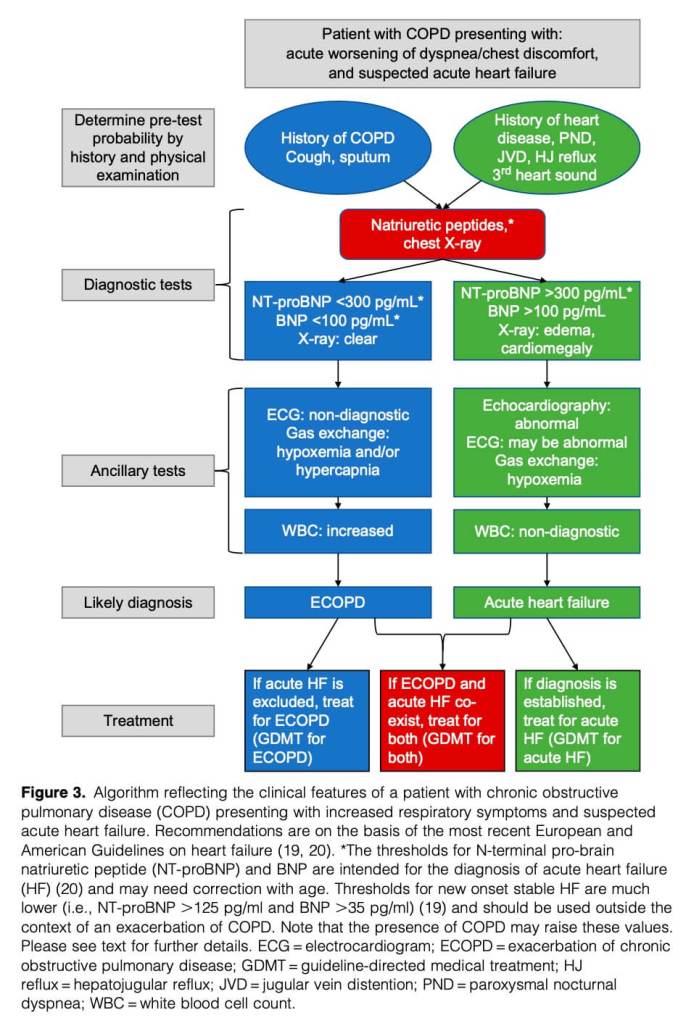
– ECI
La ECI se asocia con EA más prolongadas. El daño miocárdico es común y clínicamente significativo durante las EA, particularmente en pacientes con ECI preexistente. La EA aumenta significativamente el riesgo de infarto al miocardio y accidente cerebrovascular, no solo en los primeros 30 días después de una EA (en 4-10 veces), sino que también hasta 1 año después del evento. Un tercio de los pacientes con ECI tiene EPOC.
En pacientes con EA ambulatoria, la historia clínica y los signos de aterosclerosis sistémica o aquellos consistentes con isquemia miocárdica aguda, sugieren ECI concomitante. Los síntomas, más un electrocardiograma (ECG) anormal, apoyan la presencia de isquemia miocárdica aguda. Sin embargo, el diagnóstico de daño o infarto al miocardio requiere la elevación de la troponina en sangre, más, al menos, uno de otros factores (síntomas y/o nuevos cambios en ECG). La EPOC puede asociarse con elevaciones crónicas (usualmente estables) de las concentraciones de troponina, lo que puede aumentar más durante las EA. Dada la alta prevalencia de la ECI junto con las EA, la evaluación de la aterosclerosis y enfermedades asociadas debería ser siempre considerada.
– Arritmias
La prevalencia de arritmias cardiacas, especialmente la fibrilación auricular (FA), está aumentada en los pacientes con EPOC. Además, durante una EA, el riesgo de FA y otras arritmias se dobla. La presencia de una FA durante una EA aumenta la morbilidad y mortalidad. La FA puede sospecharse mediante la presencia del pulso irregular y se diagnostica con un ECG y monitorización cardiaca. El rol de la FA como causa de disnea aguda en pacientes con EPOC no se conoce aun.
– EP
La prevalencia de la EP en pacientes con EPOC varía entre el 3,3% al 29,4%, siendo más común en pacientes con EA atípica o sin explicación y requiere de un pronto manejo específico para mejorar los desenlaces. La EP debe considerarse en pacientes con aumento de la disnea en el contexto de factores de riesgo, como la historia de enfermedad tromboembólica venosa, hospitalizaciones por IC o cáncer.
Se ha visto que en los pacientes hospitalizados con una EA, la prevalencia global de la EP alcanza al 4-6%. Dada la alta mortalidad de la EP, la evidencia apoya la realización del angioTAC en pacientes con alta probabilidad clínica pretest de EP (puntaje de Génova de al menos 11) y frente a alguna presentación atípica de la EA, sin necesidad de la evaluación previa del dímero D. Si la probabilidad pretest es baja (puntaje de Génova <11) y el dimero D <500 ng/mL, se puede apoyar el diagnóstico de EA y evitar la realización del angioTAC. La estrategia diagnóstica frente a un paciente con sospecha de EP se muestra en la figura 4.
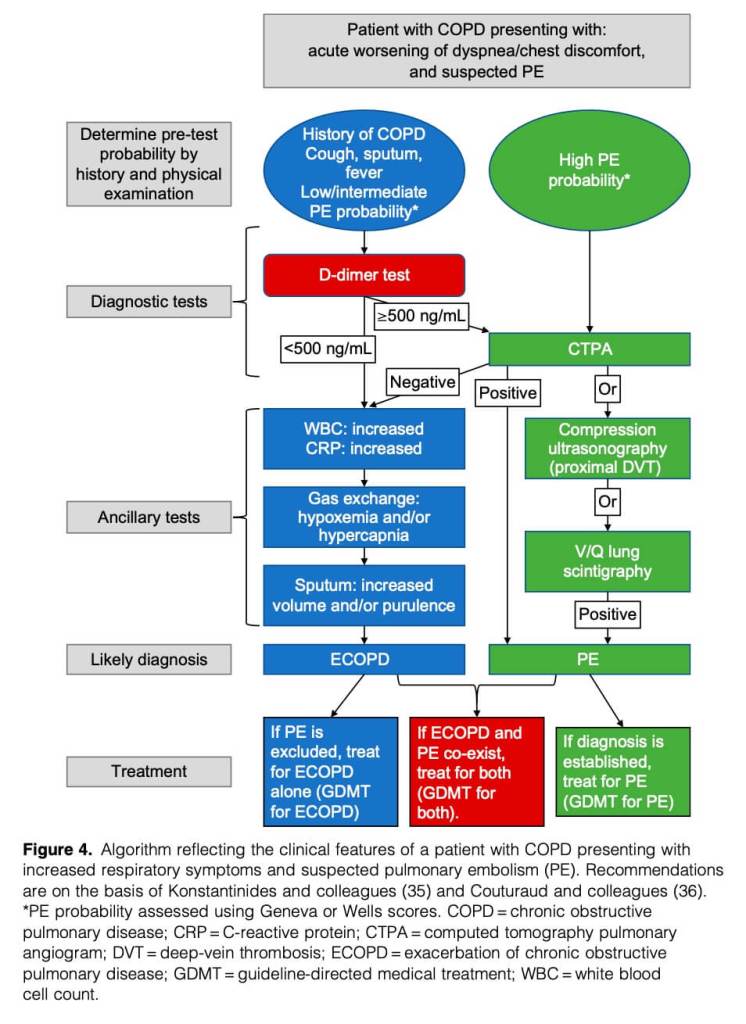
Enfermedades infecciosas
– Neumonía
En pacientes con EPOC, los síntomas de una neumonía pueden ser similares a los de una EA. El examen físico puede ayudar a diferenciarlas, con los signos de consolidación más frecuentemente presentes en las neumonías. La neumonía debe siempre ser considerada en el diagnóstico diferencial de pacientes con síntomas de una EA.
Si la evaluación clínica considera la EA como leve o moderada y no hay signos de consolidación, no se necesita realizar más exámenes para diferenciar entre ambas entidades. Pero, si el episodio es severo y/o prolongado y hay un examen torácico anormal, se requiere de buscar rápidamente el diagnóstico de neumonía. La mortalidad después de una neumonía hospitalizada es más alta que la de una EA hospitalizada. La mayoría de los pacientes sin EA severa pueden ser tratados en forma segura en base a sólo la radiografía de tórax. Valores más elevados de la PCR son más probables que apoyen el diagnóstico neumonia, particularmente de etiología bacteriana, por sobre una EA. El rol de la procalcitonina es menos claro, con evidencia que sugiere que un pacientes con baja probabilidad pretest de neumonía, los niveles bajos de procalcitonina apoyan una etiología no bacteriana del proceso.
La purulencia del esputo es un biomarcador clínico que apoya la infección bacteriana y predice el beneficio del tratamiento con antibióticos. En pacientes con EA severa o neumonía, el gram y cultivo de esputo y los exámenes moleculares pueden ayudar a guiar la terapia antibiótica.
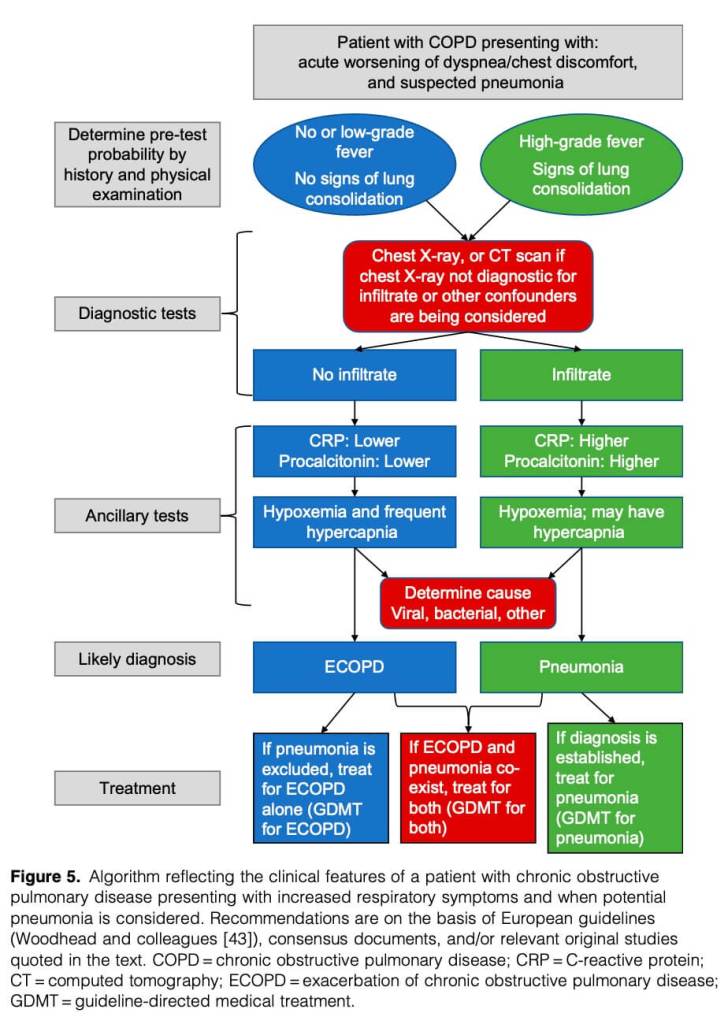
El enfoque diagnóstico para pacientes con sospecha de neumonía se ve en la figura 5.
– Bronquiectasias
La prevalencia de las bronquiectasias en pacientes con EPOC varía entre el 8% al 69%, siendo mayor en aquellos con obstrucción al flujo aéreo más severa. Los pacientes con sobreposición EPOC y bronquiectasias tienen más exacerbaciones y síntomas, mayor riesgo de neumonía y mayor mortalidad que los pacientes con los diagnósticos por separado. Este mayor riesgo de exacerbaciones puede ser debido al aislamiento más frecuente de bacterias patógenas, incluyendo la Pseudomona aeruginosa.
Los pacientes con bronquiectasias extensas pueden tener obstrucción al flujo aéreo pobremente reversible, cumpliendo los criterios de EPOC. Los criterios diagnósticos de la sobreposición EPOC/bronquiectasias incluyen la apropiada ROSE (radiología, obstrucción al flujo aéreo, síntomas y exposición). En estos pacientes, es imposible distinguir una exacerbación de las bronquiectasias de una exacerbación de la EPOC. Es recomendable realizar un TAC de tórax para excluir la presencia de bronquiectasias en pacientes EPOC con EA frecuentes.
Morbilidades inflamatorias
– Exacerbaciones del asma
La prevalencia del asma bronquial comórbida en pacientes con EPOC varía entre 3,8% a 38,8%, siendo la historia familiar, edad menor y la presencia de atopia o asma en la niñez, sugerentes de asma comórbida. Los pacientes con ambas enfermedades son más sintomáticos, tienen peor función pulmonar y mayor riesgo de exacerbaciones y hospitalizaciones, comparando con los pacientes con las enfermedades por separado.
No existen publicaciones que hayan investigado si las exacerbaciones en pacientes con asma y EPOC son diferentes a las exacerbaciones por asma o EPOC y las guías definen las exacerbaciones del asma y de la EPOC en forma similar. El manejo de las EA en los pacientes con asma concomitante es similar al manejo de las exacerbaciones del asma.
– EPI
Al igual que en la EPOC, el curso natural de las EPI (especialmente la fibrosis pulmonar idiopática [FPI]) se caracteriza por episodios de exacerbaciones, usualmente severas, las que se asocian con deterioro clínico y tienen peor pronóstico que las EA.
Algunos pacientes pueden presentar el síndrome combinado fibrosis pulmonar/enfisema. Cuando estos pacientes presentan una exacerbación, puede ser difícil diferenciar la EA de la exacerbación por la fibrosis pulmonar. La evidencia de nuevas alteraciones alveolares (opacidades en vidrio esmerilado) en el estudio de imágenes en un paciente con síntomas consistentes en una EA apoya un rol importante de una exacerbación de la fibrosis.
Morbilidades misceláneas
– Ansiedad y depresión
En pacientes con EA, la prevalencia de depresión y ansiedad varía entre 9% y 58%. Los pacientes con EPOC que tienen depresión y/o ansiedad, tienen mayor riesgo de EA y hospitalizaciones comparando con los individuos no deprimidos.
El rol causal de la ansiedad/depresión en las EA no ha sido estudiado en forma sistemática. En pacientes con EPOC que tienen ataques de pánico, la falta de aumento de la tos y esputo, en ausencia de marcadores inflamatorios u otra morbilidad que explique la disnea y la taquipnea, puede ayudar a establecer el diagnóstico.
– Neumotórax
El neumotórax es un evento potencialmente mortal que ocurre en algunos pacientes con EPOC y que se parece a una EA, por lo que requiere de un rápido diagnóstico. Las bulas subpleurales y bulas parenquimatosas son frecuentes en los hombres añosos con enfisema más severo y exposición al tabaco y/o marihuana. El diagnóstico del neumotórax se confirma generalmente con una radiografía de tórax.
– Derrame pleural
Los grandes derrame pleurales pueden contribuir al empeoramiento de la disnea en pacientes con EPOC. Si el derrame es grande y se asocia con elevación de péptidos natriuréticos, la causa más probable será cardiovascular, particularmente la IC aguda, mientras que si se asocia más bien con PCR elevada, reflejará probablemente un derrame paraneumónico o empiema. La radiografía de tórax, ultrasonografía y tomografía de tórax son útiles ara determinar la presencia, tamaño y complejidad del derrame pleural en un paciente con EA.
– Anemia
La presencia de anemia en una EA puede contribuir al aumento de la disnea.
Conclusiones
La combinación de la historia clínica y el examen físico, junto con biomarcadores clínicos actualmente existentes, pueden ayudar, en la mayoría de los pacientes con EPOC que tienen la presentación clásica de una EA, a establecer con un grado razonable de certeza la existencia de una EA. En otros pacientes, las descompensaciones agudas de morbilidades coexistentes o el desarrollo de eventos agudos, como la IC, neumonía o EP, pueden contribuir o causar esos eventos. Así, en todos los pacientes con EPOC que presentan empeoramiento de sus síntomas, sin evidencias de infección, se deberían investigar las comorbilidades frecuentes que podrían complicar dicho evento. Es extremadamente importante que los investigadores adopten un sistema más objetivo para determinar las causas de las EA, dado que los estudios, hasta ahora, podrían haber diagnosticado en forma incorrecta las EA hospitalizadas como tales, cuando, de hecho, podrían haber sido descompensaciones de comorbilidades.


Una de las comorbilidades frecuentes que acompañan a la EPOC es la insuficiencia cardíaca cuya descompensación es un verdadero desafío clínico para distinguirla de una exacerbación de la EPOC. Aún más complicado es
el diagnóstico de la insuficiencia cardíaca con función sistolica conservada. La causa más frecuente de este proceso es la afectación cardíaca de origen hipertensivo, con hipertrofia ventricular izquierda que altera las propiedades diastólicas del ventrículo y, por tanto, su presión de llenado.
Esta condición representa entre el 30 y el 50% de todos los casos de insuficiencia cardíaca.
El tratamiento de la insuficiencia cardíaca diabólica ( FEVI >50%) es el tratamiento de su etiología: la hipertensión arterial.
En la EPOC, una vez se pone en evidencia que su manejo, el tratamiento de las exacerbaciones y las comorbilidades que la acompañan require un equipo sanitario multidisciplinario.
Me gustaMe gusta
…diastólica…
Me gustaMe gusta